Services
Vestibulum ac diam sit amet quam vehicula elementum sed sit amet dui. Curabitur non nulla sit amet nisl tempus convallis quis ac lectus. Quisque velit nisi, pretium ut lacinia

Therapeutic Exersice

Electrotherapy

Aquatic Therapy

Acupuncture

Rehabilitation

Feature Box
Our Therapists
Vestibulum ac diam sit amet quam vehicula elementum sed sit amet dui. Curabitur non nulla sit amet nisl tempus convallis quis ac lectus. Quisque velit nisi, pretium ut lacinia




Home Physical Therapy
Crioconservazione
La preservazione della fertilità rappresenta una sfida importante per le pazienti oncologiche, in particolare quelle sottoposte a trattamenti gonadotossici come le chemioterapie e le radioterapie che, inevitabilmente, possono causare insufficienza ovarica prematura. In questo contesto, la crioconservazione del tessuto ovarico (OT) si è affermata come una tecnica promettente consentendo il ripristino sia della funzione endocrina che della fertilità attraverso l'autotrapianto di tessuto criopreservato e successivamente riscaldato.
La crioconservazione del tessuto ovarico si distingue per la sua capacità di essere l'unica opzione disponibile per le pazienti prepuberi o per le donne che necessitano di un trattamento oncologico immediato. Infatti, a differenza della crioconservazione di ovociti o embrioni, questa tecnica può essere eseguita senza la necessità di stimolazione ovarica, il che la rende particolarmente utile per le pazienti che non hanno tempo o possibilità di procedere con altre tecniche di riproduzione assistita.
Una delle attività di ricerca principale condotta da IVF RED è stata finalizzata al miglioramento delle tecniche di criopreservazione del tessuto ovarico.
A tal fine sono stati effettuati studi per evidenziare eventuali danni da crioconservazione su ovociti e tessuto crioconservati attraverso un procedimento di congelamento lento o vitrificazione.
Nel 2009, si è osservato che il raffreddamento lento degli ovociti in metafase II causava danni ultrastrutturali significativi, tra cui la riduzione della densità dei granuli corticali, il gonfiore del reticolo endoplasmatico liscio e danni alle membrane mitocondriali, senza però segni di apoptosi. Questo ha suggerito che tali danni potessero influire negativamente sulla competenza di sviluppo degli ovociti crioconservati [1].
A tal proposito nel 2011 uno studio ha esaminato la sensibilità degli ovociti umani al danno criogenico, confrontando quelli freschi con quelli crioconservati tramite raffreddamento lento e vitrificazione. Questo studio ha dimostrato che la vitrificazione è una tecnica più efficace nel mantenere la competenza degli ovociti [2].
Nel 2016 iniziano una serie di studi per migliorare gli attuali protocolli di vitrificazione del tessuto ovarico. Grazie a questa tecnica è stata trovata una soluzione che riduce significativamente i danni criogenici. Lo studio ha mostrato che l'aumento delle velocità di raffreddamento con azoto liquido migliora il recupero di ovociti sani, delle cellule della granulosa (GC) e delle cellule stromali (SC), preservando meglio la vitalità e la qualità del tessuto ovarico [3].
Nel 2018 è stato dimostrato che la vitrificazione con azoto liquido, abbinata alla coltura a lungo termine dopo il riscaldamento in condizioni che garantiscano una disponibilità ottimale di ossigeno nel tessuto, potrebbe consentire il recupero di un tessuto più competente, in grado di generare un numero maggiore di ovociti in metafase II [4].
Da questo momento in poi sono stati effettuati una serie di studi volti a migliorare la coltura di tessuto ovarico.
Una review del 2021 ha analizzato la letteratura relativa ai danni mitocondiali correlati al processo di crioconservazione evidenziando che il danno mitocondriale correlato allo stress ossidativo può ridurre significativamente la capacità riproduttiva delle cellule. L’analisi della letteratura ha messo in evidenza ha suggerito l'uso di antiossidanti e altre strategie per preservare la competenza riproduttiva durante il congelamento e lo scongelamento di tessuti ovarici e gameti. Questo approccio potrebbe essere cruciale per migliorare i risultati della criopreservazione [5].
Oltre a sviluppare tecniche di crioconservazione più efficaci è fondamentale garantire che il tessuto rimanga vitale durante il trasporto prima della vitrificazione.
Un recente studio del 2023 ha esplorato l'integrità dei tessuti ovarici prelevati da bovini prepuberi, conservati a temperatura ipotermica (4°C) fino a 72 ore prima del congelamento. I risultati suggeriscono che anche un trasporto a basse temperature per un periodo prolungato non compromette la qualità del tessuto, il che può facilitare l’accesso a queste tecniche, anche in contesti in cui è necessario il trasporto del tessuto verso centri specializzati [6].
La qualità degli ovociti diminuisce con l'età materna e questo influisce anche sulla loro criosuscettibilità. Uno studio del 2024 ha evidenziato che gli ovociti di topi anziani avevano una maggiore suscettibilità ai danni da vitrificazione rispetto agli ovociti più giovani, specialmente quando questi ultimi venivano raccolti tramite superovulazione piuttosto che maturazione in vitro. Ciò suggerisce che la vitrificazione potrebbe essere meno efficace nelle donne anziane, richiedendo strategie di preservazione specifiche per gruppi di età diverse [7].
Conclusione
La crioconservazione del tessuto ovarico rappresenta un'area di ricerca in rapida evoluzione, con nuove tecniche e approcci che cercano di minimizzare i danni cellulari e migliorare i risultati della preservazione della fertilità. Sebbene la vitrificazione stia guadagnando terreno come tecnica di riferimento, restano ancora numerose sfide da superare, specialmente per quanto riguarda l'ottimizzazione dei protocolli per diversi tipi di tessuti e per pazienti di diverse età. La ricerca continua è fondamentale per perfezionare queste tecniche e offrire soluzioni sicure ed efficaci per le pazienti che desiderano preservare la propria fertilità.
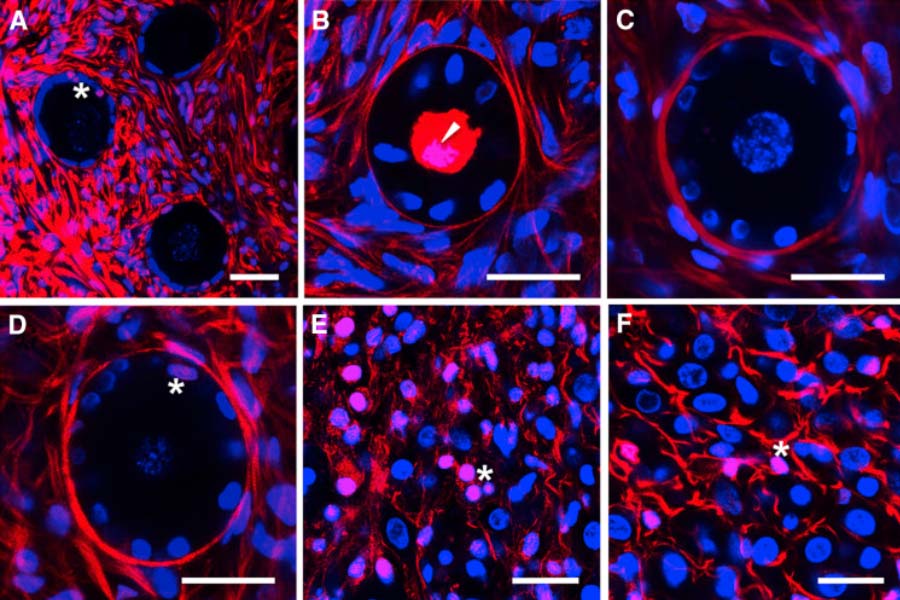
Figura 1 . Micrografie confocali rappresentative della vitalità del tessuto ovarico (rosso : sonda rosso lontano vivo-morto; blu : nuclei colorati con Hoechst 33342).
Referenze:
[1]Gualtieri R, Iaccarino M, Mollo V, Prisco M, Iaccarino S, Talevi R. Slow cooling of human oocytes: ultrastructural injuries and apoptotic status. Fertil Steril. 2009 Apr;91(4):1023-34. doi: 10.1016/j.fertnstert.2008.01.076. Epub 2008 Mar 25. PMID: 18367177.
[2] Gualtieri R, Mollo V, Barbato V, Fiorentino I, Iaccarino M, Talevi R. Ultrastructure and intracellular calcium response during activation in vitrified and slow-frozen human oocytes. Hum Reprod. 2011 Sep;26(9):2452-60. doi: 10.1093/humrep/der210. Epub 2011 Jun 29. PMID: 21715449.
[3]Talevi R, Barbato V, Fiorentino I, Braun S, De Stefano C, Ferraro R, Sudhakaran S, Gualtieri R. Successful slush nitrogen vitrification of human ovarian tissue. Fertil Steril. 2016 Jun;105(6):1523-1531.e1. doi: 10.1016/j.fertnstert.2016.01.043. Epub 2016 Feb 19. PMID: 26902858.
[4] Barbato V, Gualtieri R, Capriglione T, Pallotta MM, Braun S, Di Nardo M, Costanzo V, Ferraro R, Catapano G, Talevi R. Slush nitrogen vitrification of human ovarian tissue does not alter gene expression and improves follicle health and progression in long-term in vitro culture. Fertil Steril. 2018 Dec;110(7):1356-1366. doi: 10.1016/j.fertnstert.2018.08.020. PMID: 30503135.
[5] Gualtieri R, Kalthur G, Barbato V, Di Nardo M, Adiga SK, Talevi R. Mitochondrial Dysfunction and Oxidative Stress Caused by Cryopreservation in Reproductive Cells. Antioxidants (Basel). 2021 Feb 24;10(3):337. doi: 10.3390/antiox10030337. PMID: 33668300; PMCID: PMC7996228.
[6] Amonkar DDB, Genovese V, De Gregorio V, Travaglione A, Uppangala S, Vani Lakshmi R, Kalthur G, Gualtieri R, Talevi R, Adiga SK. Impact of prepubertal bovine ovarian tissue pre-freeze holding duration on follicle quality. Reprod Biol. 2023 Sep;23(3):100794. doi: 10.1016/j.repbio.2023.100794. Epub 2023 Jul 31. PMID: 37531931.
[7] Daddangadi A, Uppangala S, Kabekkodu SP, Khan G N, Kalthur G, Talevi R, Adiga SK. Advanced Maternal Age Affects the Cryosusceptibility of Ovulated but not In Vitro Matured Mouse Oocytes. Reprod Sci. 2024 May;31(5):1420-1428. doi: 10.1007/s43032-024-01462-6. Epub 2024 Jan 31. PMID: 38294668; PMCID: PMC11090971.



